
Chirurgische Gesichtsmaske 6002-2 EO sterilisiert
Materialien
• Oberfläche: 60 g Vliesstoff
• Zweite Schicht: 45 g Heißluftbaumwolle
• Dritte Schicht: 50 g FFP2-Filtermaterial
• Innere Schicht: 30 g PP-Vliesstoff
Zulassungen und Standards
• EU-Norm: EN14683:2019 Typ IIR
• EU-Norm: EN149:2001 FFP2-Level
• Lizenz zur Herstellung von Industrieprodukten
Gültigkeit
• 2 Jahre
Verwendung für
• Dient zum Schutz vor Partikeln, die bei der Verarbeitung von Erz, Kohle, Eisenerz, Mehl, Metall, Holz, Pollen und bestimmten anderen Materialien entstehen, z. B. beim Schleifen, Sandstrahlen, Reinigen, Sägen, Verpacken oder Verarbeiten.
Lagerbedingungen
• Luftfeuchtigkeit <80 %, gut belüftete und saubere Innenumgebung ohne korrosive Gase
Ursprungsland
• In China hergestellt
| Beschreibung | Kasten | Karton | Bruttogewicht | Kartongröße |
| Chirurgische Gesichtsmaske 6002-2 EO sterilisiert | 20 Stück | 400 Stück | 9kg/Karton | 62x37 x38cm |
Dieses Produkt entspricht den Anforderungen der EU-Verordnung (EU) 2016/425 für persönliche Schutzausrüstung und erfüllt die Anforderungen der europäischen Norm EN 149:2001+A1:2009. Gleichzeitig entspricht es den Anforderungen der EU-Verordnung (EU) MDD 93/42/EWG über Medizinprodukte und erfüllt die Anforderungen der europäischen Norm EN 14683-2019+AC:2019.
Benutzerhinweise
Die Maske muss für den vorgesehenen Einsatzzweck geeignet ausgewählt werden. Eine individuelle Risikobewertung ist erforderlich. Überprüfen Sie die Atemschutzmaske auf Beschädigungen und sichtbare Mängel. Überprüfen Sie das noch nicht abgelaufene Verfallsdatum (siehe Verpackung). Überprüfen Sie die für das verwendete Produkt und dessen Konzentration geeignete Schutzklasse. Verwenden Sie die Maske nicht, wenn ein Defekt vorliegt oder das Verfallsdatum überschritten ist. Die Nichtbeachtung aller Anweisungen und Einschränkungen kann die Wirksamkeit dieser partikelfiltrierenden Halbmaske erheblich beeinträchtigen und zu Krankheit, Verletzung oder Tod führen. Eine richtig ausgewählte Atemschutzmaske ist unerlässlich. Vor dem Einsatz am Arbeitsplatz muss der Träger vom Arbeitgeber in der korrekten Verwendung der Atemschutzmaske gemäß den geltenden Sicherheits- und Gesundheitsstandards geschult werden.
Anwendungsgebiete
Dieses Produkt ist auf chirurgische Eingriffe und andere medizinische Umgebungen beschränkt, in denen Infektionserreger vom Personal auf Patienten übertragen werden. Die Barriere soll auch den Ausfluss von Infektionserregern aus Mund und Nase von asymptomatischen Trägern oder klinisch symptomatischen Patienten wirksam reduzieren und in anderen Umgebungen vor festen und flüssigen Aerosolen schützen.
Methode verwenden
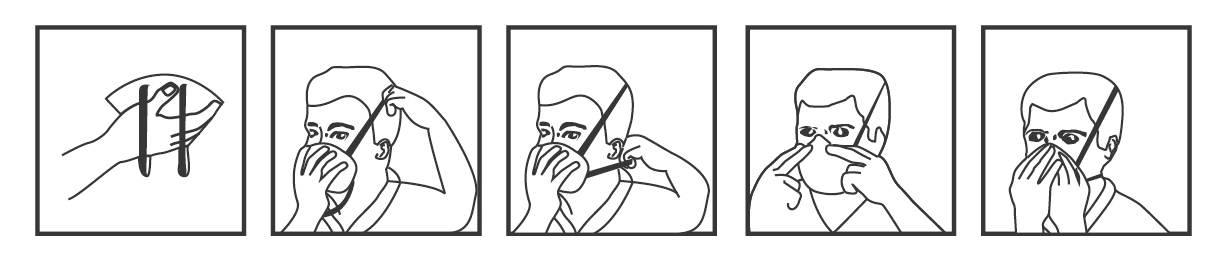
1. Halten Sie die Maske mit dem Nasenclip nach oben in der Hand. Lassen Sie das Kopfband frei hängen.
2. Positionieren Sie die Maske unter dem Kinn und bedecken Sie Mund und Nase.
3. Ziehen Sie das Kopfgeschirr über den Kopf und positionieren Sie es hinter dem Kopf. Passen Sie die Länge des Kopfgeschirrs mit der verstellbaren Schnalle an, damit es sich so angenehm wie möglich anfühlt.
4. Drücken Sie den weichen Nasenclip fest an die Nase.
5. Um den Sitz zu prüfen, halten Sie beide Hände über die Maske und atmen Sie kräftig aus. Wenn Luft um die Nase strömt, ziehen Sie den Nasenclip fest. Tritt am Rand Luft aus, positionieren Sie die Kopfbänderung für einen besseren Sitz. Überprüfen Sie die Dichtheit erneut und wiederholen Sie den Vorgang, bis die Maske richtig abdichtet.
Hintergrund
Medizinische Geräte werden auf verschiedene Weise sterilisiert, unter anderem mit feuchter Hitze (Dampf), trockener Hitze, Bestrahlung, Ethylenoxidgas, verdampftem Wasserstoffperoxid und anderen Sterilisationsmethoden (z. B. Chlordioxidgas, verdampfter Peressigsäure und Stickstoffdioxid).
Desinfektion ist die antimikrobielle Reduzierung der Anzahl lebensfähiger Mikroorganismen auf ein zuvor festgelegtes Niveau für die beabsichtigte weitere Handhabung oder Verwendung. Sterilisation ist ein definierter Prozess, der dazu dient, eine Oberfläche oder ein Produkt von lebensfähigen Organismen, einschließlich Bakteriensporen, zu befreien. Sie dient häufig auch der Aufrechterhaltung des sterilen Zustands.
Gründe für die Verwendung von Ethylenoxid (EO)
Medizinische Geräte werden auf verschiedene Arten sterilisiert, unter anderem mit feuchter Hitze (Dampf), trockener Hitze, Bestrahlung, Ethylenoxidgas, verdampftem Wasserstoffperoxid und anderen Sterilisationsmethoden (z. B. Chlordioxidgas, verdampfter Peressigsäure und Stickstoffdioxid). Die Ethylenoxid-Sterilisation ist ein wichtiges Sterilisationsverfahren, das Hersteller häufig zur Gewährleistung der Sicherheit medizinischer Geräte einsetzen.
Ethylenoxid ist ein brennbares, farbloses Gas, das zur Herstellung anderer Chemikalien verwendet wird, die in einer Reihe von Produkten wie Textilien, Kunststoffen, Reinigungsmitteln und Klebstoffen Verwendung finden. Ethylenoxid wird auch zur Sterilisation von Geräten und Kunststoffprodukten verwendet, die nicht mit Dampf, Gammastrahlen oder anderen Sterilisationsmitteln sterilisiert werden können, wie z. B. medizinische Geräte.
Das Produkt wurde auf Sterilität getestet
Die Population lebensfähiger Mikroorganismen auf oder im Produkt wurde gemäß ISO 11737-2:2009 getestet.
Entnehmen Sie 10 Proben aus der Packung und beimpfen Sie jede Probe nach dem aseptischen Schneiden in 100 ml flüssiges Thioglykolatmedium (FTM) und 100 ml Trypticase-Soja-Bouillon (TSB). Das FTM wird für 14 Tage in einen Inkubator bei 35 °C und die TSB für 25 °C gestellt. Geben Sie 80 KBE Staphylococcus aureus zum Kulturmedium hinzu und kultivieren Sie die Probe fünf Tage lang im Inkubator als positive Kontrolle. Für die negative Kontrolle werden 100 ml FTM und 100 ml TSB 14 Tage lang in Inkubatoren kultiviert. Beobachten Sie täglich das Wachstum der Mikroorganismen.
Die Ergebnisse zeigten, dass in den Testproben keine Freisetzungen festgestellt wurden, die das Wachstum von Mikroorganismen beeinträchtigen. Der Testartikel erfüllte die Kriterien, und die Testergebnisse sind gültig.
Aufgrund der obigen Ergebnisse kann der Schluss gezogen werden, dass die Testproben unter den Versuchsbedingungen steril sind.











