
Chirurgische Gesichtsmaske 6003-2 EO sterilisiert
Materialien
• Oberfläche: 60 g Vliesstoff
• Zweite Schicht: 45 g Heißluftbaumwolle
• Dritte Schicht: 50 g FFP2-Filtermaterial
• Innere Schicht: 30 g PP-Vliesstoff
Zulassungen und Standards
• EU-Norm: EN14683:2019 Typ IIR
• EU-Norm: EN149:2001 FFP2-Level
• Lizenz zur Herstellung von Industrieprodukten
Gültigkeit
• 2 Jahre
Verwendung für
• Dient zum Schutz vor Partikeln, die bei der Verarbeitung von Erz, Kohle, Eisenerz, Mehl, Metall, Holz, Pollen und bestimmten anderen Materialien entstehen, z. B. beim Schleifen, Sandstrahlen, Reinigen, Sägen, Verpacken oder Verarbeiten.
Lagerbedingungen
• Luftfeuchtigkeit <80 %, gut belüftete und saubere Innenumgebung ohne korrosive Gase
Ursprungsland
• In China hergestellt
| Beschreibung | Kasten | Karton | Bruttogewicht | Kartongröße |
| Chirurgische Gesichtsmaske 6003-2 EO sterilisiert | 20 Stück | 400 Stück | 9kg/Karton | 62x37 x38cm |
Dieses Produkt entspricht den Anforderungen der EU-Verordnung (EU) 2016/425 für persönliche Schutzausrüstung und erfüllt die Anforderungen der europäischen Norm EN 149:2001+A1:2009. Gleichzeitig entspricht es den Anforderungen der EU-Verordnung (EU) MDD 93/42/EWG über Medizinprodukte und erfüllt die Anforderungen der europäischen Norm EN 14683-2019+AC:2019.
Benutzerhinweise
Die Maske muss für den vorgesehenen Einsatzzweck geeignet ausgewählt werden. Eine individuelle Risikobewertung ist erforderlich. Überprüfen Sie die Atemschutzmaske auf Beschädigungen und sichtbare Mängel. Überprüfen Sie das noch nicht abgelaufene Verfallsdatum (siehe Verpackung). Überprüfen Sie die für das verwendete Produkt und dessen Konzentration geeignete Schutzklasse. Verwenden Sie die Maske nicht, wenn ein Defekt vorliegt oder das Verfallsdatum überschritten ist. Die Nichtbeachtung aller Anweisungen und Einschränkungen kann die Wirksamkeit dieser partikelfiltrierenden Halbmaske erheblich beeinträchtigen und zu Krankheit, Verletzung oder Tod führen. Eine richtig ausgewählte Atemschutzmaske ist unerlässlich. Vor dem Einsatz am Arbeitsplatz muss der Träger vom Arbeitgeber in der korrekten Verwendung der Atemschutzmaske gemäß den geltenden Sicherheits- und Gesundheitsstandards geschult werden.
Anwendungsgebiete
Dieses Produkt ist auf chirurgische Eingriffe und andere medizinische Umgebungen beschränkt, in denen Infektionserreger vom Personal auf Patienten übertragen werden. Die Barriere soll auch den Ausfluss von Infektionserregern aus Mund und Nase von asymptomatischen Trägern oder klinisch symptomatischen Patienten wirksam reduzieren und in anderen Umgebungen vor festen und flüssigen Aerosolen schützen.
Methode verwenden
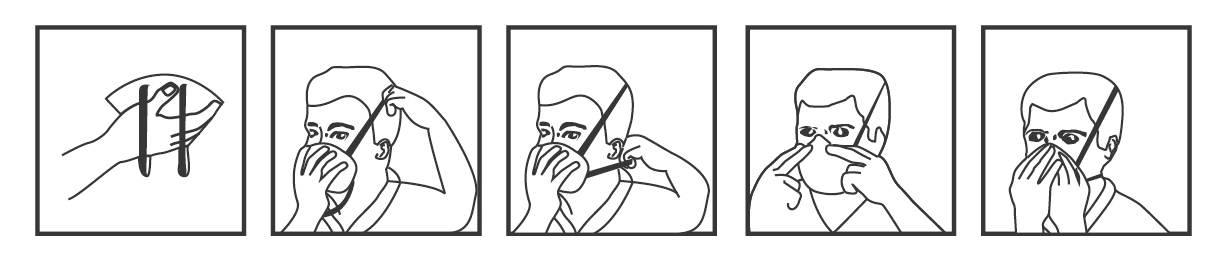
1. Halten Sie die Maske mit dem Nasenclip nach oben in der Hand. Lassen Sie das Kopfband frei hängen.
2. Positionieren Sie die Maske unter dem Kinn und bedecken Sie Mund und Nase.
3. Ziehen Sie das Kopfgeschirr über den Kopf und positionieren Sie es hinter dem Kopf. Passen Sie die Länge des Kopfgeschirrs mit der verstellbaren Schnalle an, damit es sich so angenehm wie möglich anfühlt.
4. Drücken Sie den weichen Nasenclip fest an die Nase.
5. Um den Sitz zu prüfen, halten Sie beide Hände über die Maske und atmen Sie kräftig aus. Wenn Luft um die Nase strömt, ziehen Sie den Nasenclip fest. Tritt am Rand Luft aus, positionieren Sie die Kopfbänderung für einen besseren Sitz. Überprüfen Sie die Dichtheit erneut und wiederholen Sie den Vorgang, bis die Maske richtig abdichtet.
6003-2 EO sterilisiert erfüllt die Norm EN14683. Zu den Testpunkten gehören ein Test der bakteriellen Filtrationseffizienz (BFE), ein Differenzdrucktest und ein Test zur Penetration mit synthetischem Blut.
Test der bakteriellen Filtrationseffizienz (BFE)
Zweck
Zur Bewertung der bakteriellen Filtrationseffizienz (BFE) einer Maske.
Berechnung
Die Zählung der Testproben und Positivkontrollen auf jeder der sechs Platten wird gemäß den Angaben des Anderson-Probenehmerherstellers summiert. Die prozentuale Filtrationseffizienz wird wie folgt berechnet:
BFE = (CT) / C × 100
T ist die Gesamtkeimzahl der Testprobe.
C ist der Mittelwert der Gesamtkeimzahl für die beiden positiven Kontrollen.
Differenzdruckprüfung
1. Zweck
Ziel des Tests war es, den Differenzdruck von Masken zu messen.
2.Beispielbeschreibung
Beispielbeschreibung: Einwegmaske mit Ohrschlaufe
3.Testmethode
EN 14683:2019+AC:2019(E) Anhang C
4.Geräte und Materialien
Differenzdruckprüfgerät
5. Prüfling
5.1 Prüflinge bestehen aus vollständigen Masken oder werden aus Masken ausgeschnitten. Jeder Prüfling muss fünf verschiedene kreisförmige Prüfbereiche mit einem Durchmesser von 2,5 cm bieten.
5.2 Vor der Prüfung alle Prüflinge mindestens 4 Stunden lang bei (21±5)℃ und (85±5)% relativer Luftfeuchtigkeit konditionieren
6. Verfahren
6.1 Ohne eingelegte Probe wird der Halter geschlossen und das Differenzdruckmessgerät auf Null gestellt. Die Pumpe wird gestartet und der Luftstrom auf 8 l/min eingestellt.
6.2 Die vorbehandelte Probe wird über die Öffnung gelegt (Gesamtfläche 4,9 cm², Testflächendurchmesser 25 mm) und festgeklemmt, um Luftlecks zu minimieren.
6.3 Aufgrund des vorhandenen Ausrichtungssystems sollte der getestete Bereich der Probe perfekt in einer Linie und quer zum Luftstrom liegen.
6.4 Der Differenzdruck wird direkt abgelesen.
6.5 Das in den Schritten 6.1–6.4 beschriebene Verfahren wird an 5 verschiedenen Bereichen der Maske durchgeführt und die Messwerte gemittelt.
Synthetischer Blutpenetrationstest
1. Zweck
Zur Bewertung der Widerstandsfähigkeit von Masken gegen das Eindringen einer festen Menge synthetischen Blutes mit hoher Geschwindigkeit.
2.Beispielbeschreibung
Beispielbeschreibung: Einwegmaske mit Ohrschlaufe
3.Testmethode
ISO 22609:2004
4.Ergebnisse:
Gemäß ISO 22609 wird für einen normalen Einzelstichprobenplan eine akzeptable Qualitätsgrenze von 4,0 % erreicht, wenn ≥29 von 32 Testartikeln ein positives Ergebnis aufweisen.









